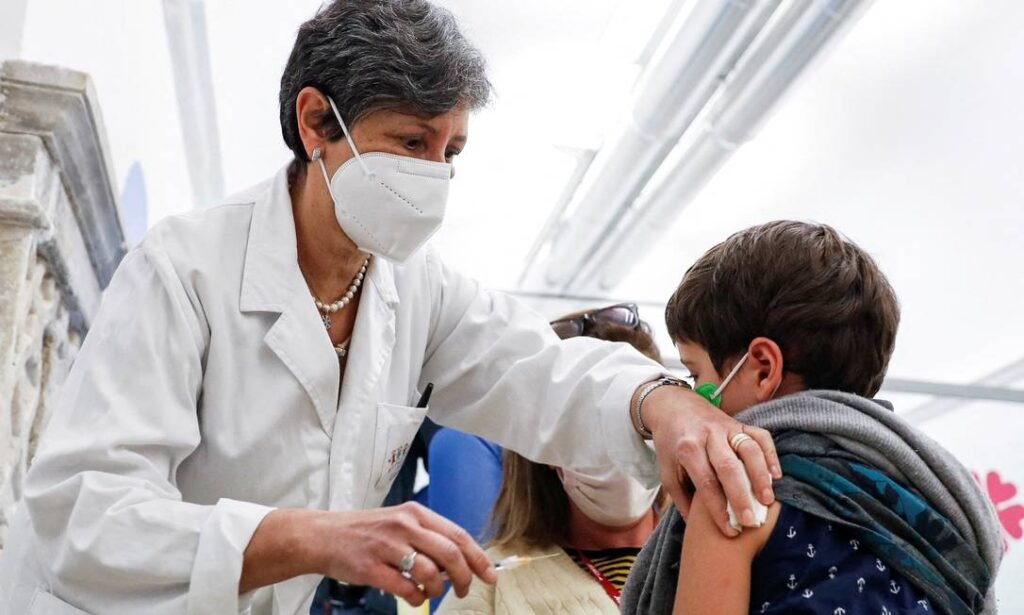
A Agência Nacional de Vigilância Sanitária (Anvisa) incluiu crianças de 5 a 11 anos na bula da vacina da Pfizer contra a Covid-19. A decisão foi anunciada em reunião virtual e uma resolução deve ser publicada em edição extra do Diário Oficial da União (DOU) ainda nesta quinta-feira.
A composição da vacinas das crianças é diferente da dos adultos e corresponde a um terço da dose. Para diferenciá-las, os frascos terão as cores laranja e roxa, respectivamente. O imunizante infantil poderá ser armazenado por 10 semanas de 2°C a 8°C contra quatro semanas da destinada a adultos.
— Não há relato de nenhum evento adverso sério, de preocupação, não há relato relacionado a casos muito graves ou mortalidade por conta da vacinação comparado com placebo. Esse perfil de segurança é importante e a gente sabe que essa é uma das maiores preocupações na hora de extrapolar uma vacina para a população pediátrica — afirmou o gerente-geral de Medicamentos e Produtos Biológicos (GGMED) da Anvisa, Gustavo Mendes.
Quem completar 12 anos entre a primeira e a segunda dose deve completar o ciclo de imunização com a dose reduzida. Na avaliação da Anvisa e de especialistas, os riscos da vacinação infantil superam possíveis riscos. Não há votação, já que o imunizante tem registro de uso definitivo no Brasil. O órgão acata a decisão da área técnica.
Haverá monitoramento de farmacovigilãncia após a administração das doses. Durante a apresentação, Mendes citou que a miocardite e a pericardite são pontios de análise, mas representam apenas 0,007% dos casos.
Ainda não há data para a vacinação da faixa etária começar. Como O GLOBO mostrou, o Ministério da Saúde ainda não reservou doses para o grupo.
A decisão contou com apoio técnico das sociedades brasileiras de Pneumologia e Tisiologia (SBPT), de Pediatria (SBP), de Infectologia (SBI) e de Imunologia (SBI).
Fonte: globo.com